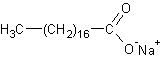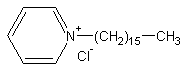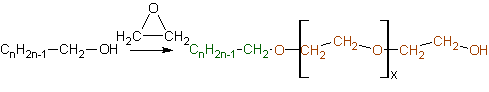Поверхностно-активные вещества — различия между версиями
VEK (обсуждение | вклад) (→Классификация ПАВ) |
|||
| Строка 7: | Строка 7: | ||
== Классификация ПАВ == | == Классификация ПАВ == | ||
| − | Различают | + | Различают [[катион]]огенные, [[анион]]огенные, и неионогенные ПАВ. В первых двух случаях молекулы ПАВ [[электролитическая диссоциация|диссоциируют]] в растворе на ионы. Адсорбируются на границе раздела фаз, соответственно, у анионогенных ПАВ (пример- мыла, R-COONa, адсорбируются R-COO<sup>-</sup>), анионы, у катионогенных- катионы (пример- хлорид цетилпиридиния Py-(CH<sub>2</sub>)<sub>16</sub>-CH<sub>3</sub>*HCl, адсорбируется Py<sup>(+)</sup>-(CH<sub>2</sub>)<sub>16</sub>-CH<sub>3</sub>). Неионогенные ПАВ- недиссоциирующие молекулы, чаще всего это продукт взаимодействия высшего спирта с несколькими молекулами [[этиленоксид]]а. В такой молекуле неполярным "хвостом" является углеводородный радикал, а полярным- олигомер этиленоксида. |
| + | |||
| + | |||
| + | *Олеат натрия | ||
| + | [[Изображение:олеат_натрия.gif]] | ||
| + | |||
| + | *Хлорид цетилпиридиния | ||
| + | [[Изображение:цетилпиридиния_хлорид.gif]] | ||
| + | |||
| + | *Схема синтеза неионогенного ПАВ | ||
| + | [[Изображение:синтез_Н-ПАВ.gif]] | ||
[[Категория:Вещества]] | [[Категория:Вещества]] | ||
[[Категория:Аббревиатуры]] | [[Категория:Аббревиатуры]] | ||
Версия 22:27, 17 февраля 2008
Поверхностно-активные вещества (ПАВ)- вещества, добавление которых к жидкости снижает её поверхностное натяжение.
Молекулы ПАВ должны быть дифильными, т.е. проявлять сродство как к полярным, так и к неполярным средам. Классическим примером являются натриевые или кальциевые соли высших жирных кислот, где длинный углеводородный радикал имеет сродство к жирам, а карбоксильная группа- к воде. (т.к. сами эти кислоты очень плохо растворимы в воде, то используются Na- и K- соли, растворимость которых выше)
Снижение поверхностного натяжения происходит за счёт адсорбции молекул ПАВ на границе двух сред жидкость-жидкость(вода/эфир) или жидкость-газ(спирт/воздух). Адсорбция ПАВ происходит самопроизвольно, т.е. изменение энергии Гиббса для этого процесса отрицательно (dG<0).
Классификация ПАВ
Различают катионогенные, анионогенные, и неионогенные ПАВ. В первых двух случаях молекулы ПАВ диссоциируют в растворе на ионы. Адсорбируются на границе раздела фаз, соответственно, у анионогенных ПАВ (пример- мыла, R-COONa, адсорбируются R-COO-), анионы, у катионогенных- катионы (пример- хлорид цетилпиридиния Py-(CH2)16-CH3*HCl, адсорбируется Py(+)-(CH2)16-CH3). Неионогенные ПАВ- недиссоциирующие молекулы, чаще всего это продукт взаимодействия высшего спирта с несколькими молекулами этиленоксида. В такой молекуле неполярным "хвостом" является углеводородный радикал, а полярным- олигомер этиленоксида.
- Олеат натрия
- Хлорид цетилпиридиния
- Схема синтеза неионогенного ПАВ